Responsable/s del laboratorio
intro
Nuestro grupo tiene como objetivo desvelar la estructura de las máquinas celulares para generar conocimiento sobre el mecanismo funcional de las macromoléculas y ayudar al desarrollo de aplicaciones biomédicas. Para ello utilizamos la criomicroscopía electrónica (cryo-EM) y la cristalografía de rayos X, que ambas aportan información a resolución atómica, combinada con otras técnicas biofísicas y bioquímicas. Esta metodología integradora se aplica al estudio de procesos celulares esenciales como la transcripción del genoma, la reparación del ADN, la integración de retrotransposones y la división celular.

Transcripción del genoma
La transferencia de información genética codificada en el ADN es el principal determinante de la expresión génica. Las alteraciones en este proceso tienen un impacto significativo en la homeostasis celular y están directamente relacionadas con el desarrollo de enfermedades. Las ARN polimerasas transcriben la información genética del ADN al ARN, catalizando la adición de nucleótidos complementarios a la hebra molde del ADN. Los eucariotas possen tres ARN polimerasas diferentes, cada una de las cuales transcribe un conjunto específico de genes. Nuestro grupo está centrado en el estudio de la ARN polimerasa I y diversos factores de transcripción que regulan la expresión génica. Para más detalles, pinchar [aquí].

Detección y reparación de lesiones en el ADN
Las lesiones en el ADN amenazan la vida celular y deben repararse para mantener la integridad del genoma. La transcripción es particularmente sensible a las lesiones en el ADN y, por lo tanto, está relacionada con la reparación del ADN. Diferentes lesiones provocan el bloqueo de las ARN polimerasas, lo que activa el reclutamiento de factores de reparación del ADN, incluidas las endonucleasas XPF y XPG para eliminar la lesión. Las alteraciones en estos factores de reparación se asocian con trastornos genéticos como la xerodermia pigmentosa y el síndrome de Cockayne. Nuestro grupo está centrado en el estudio de la detección de lesiones por las ARN polimerasas y la eliminación del ADN dañado por la XPG. Para más detalles, pinchar [aquí].

Integración dirigida del ADN
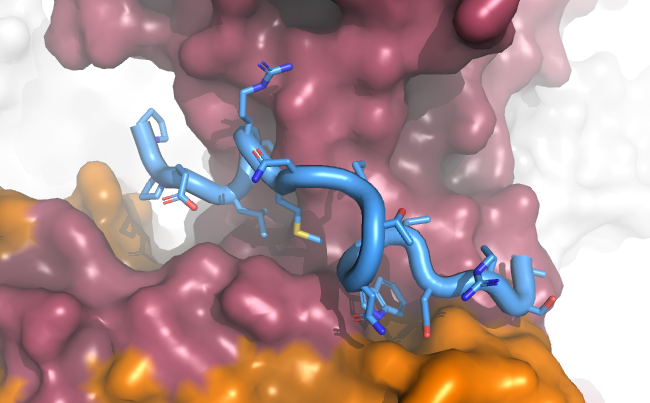
Los transposones son secuencias de ADN que pueden cambiar su posición dentro de los genomas. Su mobilidad impulsa el desarrollo de nuevas funciones celulares, pero también puede producir mutaciones perjudiciales. Para minimizar los efectos nocivos, los retrotransposones se insertan en regiones seguras del genoma mediante la unión de su integrasa a proteínas que actúan sobre la cromatina, como las ARN polimerasas. Para más detalles, pinchar [aquí].
División celular bacteriana
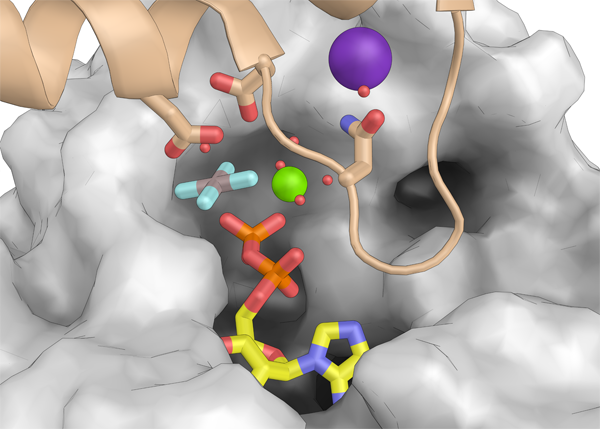
La división celular es un proceso biológico esencial que permite la propagación de los organismos vivos. La división bacteriana implica el ensamblaje de proteínas en el divisoma, que coordina la invaginación de la membrana y la síntesis de la pared celular, dando lugar finalmente a dos células hijas. Por ello, las proteínas de la división celular bacteriana son dianas para el descubrimiento de nuevos antibióticos, necesarios para combatir patógenos bacterianos resistentes. Nos centramos en el estudio de FtsZ, un homólogo ancestral de la tubulina que desempeña un papel central en la división celular bacteriana. Para más detalles, pinchar [aquí].
Miembros
| Carlos Fernández Tornero |
| Sonia Huecas Gayo |
| Federico Martin Ruiz |
| Tommy Pascal Darriere |
| Alicia Santos Gonzalez de Aledo |
| Jimena Fornas de la Rosa |

Fondos
2021-2024. PID2020-116722GB-I00. MICINN [IP]
2022-2024. Colaboración industrial con PharmaMar [IP]
2018-2021. BFU2017-87397-P. MICINN [IP]
2020-2021. 2020AEP152. CSIC [PI]
2015-2018. Fundación Ramón Areces [PI]
2014-2017. BFU2013-48374-P. MICINN [IP]
2011-2013. BFU2010-16336. MICINN [IP]
2011-2018. Colaboración industrial con PharmaMar [IP]
2010-2012. EIC-EMBL-2011-0076. MICINN [IP]
2010-2011. 200920I077. CSIC [IP]
2018-2022. Agence Nationale de la Recherche (Francia). [Líder de grupo]
2021-2022. EQC2021-006930-P. MICINN [Líder de grupo]
2020-2022. RED2018-102467-T. MICINN [Líder de grupo]
2016-2017. BFU2015-71978-REDT. MICINN [Líder de grupo]
2014-2015. CSIC13-4E-1700. MICINN [Líder de grupo]
Más información
Otras publicaciones
Fernández-Tornero C. (2021) Hibernación molecular. Article & interview in SEBBM Section 'Nuestros Científicos'
Fernández-Tornero C. (2017) Dime con quién andan tus proteínas y te diré qué hacen tus células. Huffington Post – 21 marzo
Fernández-Tornero C. (2013) Viaje al centro de la célula. Huffington Post – 31 octubre (Portada)
Fernández-Tornero C. (2014) La síntesis del ARN: un proceso en el centro de la vida. Boletín de la Institución Libre de Enseñanza 95-96:77-87
Fernandez-Tornero C. (2010) Nobel Prize in Chemistry 2009: atomic structure of the cellular machinery for protein synthesis. Anales de la Real Academia Nacional de Farmacia 76:119-136
Selección de referencias en los medios de comunicación
http://www3.radioecca.org/radio/carta/lo-nuestro/84790552
https://www.larazon.es/sociedad/20220323/zstidhycwvgadduj2vz7tcwnam.html
https://www.efe.com/efe/espana/efefuturo/-/50000905-3725429
https://www.sciencedaily.com/releases/2018/08/180822164205.htm
Redes
RNA Life Network [Grupo asociado]
LifeHUB Network [Grupo asociado]
Alumni
Srdja Drakulic, Postdoc (2017-2019)
Mercedes Spínola-Amilibia, Postdoc (2017)
Rocío González-Corrochano, Postdoc (2011-2016)
Eva Torreira, Postdoc (2011-2016)
Nicholas M. I. Taylor, Postdoc (2011-2012)
Adrián Plaza-Pegueroles, PhD Student (2019-2024)
Phong Q. Nguyen, PhD Student (2019-2022)
Marta Sanz-Murillo, PhD Student (2014-2019)
Jaime A. Louro, PhD Student (2011-2016)
Jimena Fornás de la Rosa (2023)
Héctor Leal Lasalle (2022)
Carolina Muñoz Núñez (2021)
Erica González Castro (2020)
Carla Gracia Paricio (2020)
Alicia Santos González de Aledo (2018-2019)
Álvaro Ras Carmona (2018)
Carolina Correa Maté (2017-2018)
Carlos Pardo Hernández (2017)
Álvaro de la Gándara (2017)
Paula García Trapote (2015-2016)
Nuria Castillo Tutor (2011-2015)
Pablo Saralegui (2011)
Marcel Rösinger (2010-2011)

